Neural correlates underlying state anxiety alterations following sleep deprivation: insights from frontal alpha asymmetry and phase-amplitude coupling
睡眠剝奪後狀態焦慮改變的神經相關性:來自額葉alpha不對稱與相位-振幅耦合的發現
- IF: Unknown (Pending)
- SCI
摘要
- 研究主題: 探討一晚完全睡眠剝奪對狀態焦慮(state anxiety)的影響,以及其相關的靜息態腦神經指標改變,包括額葉 alpha 波不對稱(Frontal Alpha Asymmetry, FAA)與相位-振幅耦合(Phase-Amplitude Coupling, PAC)。
- 實驗設計:
- 招募健康年輕成人進行正常睡眠 (NS) 與 24 小時睡眠剝奪 (SD) 兩種情境比較(順序隨機交叉)。
- 隔日早晨記錄眼睛張開的靜息態 EEG 5分鐘並評估狀態焦慮量表(SAI),以比較睡眠剝奪前後差異。
- 主要發現:
- 與充足睡眠相比,一晚睡眠剝奪後受試者的狀態焦慮顯著升高。
- 大腦靜息態 EEG 頻譜功率在 delta / theta / alpha / beta 波段皆全面上升。
- 額葉 alpha 波不對稱指標顯著下降(左側化)。
- delta–beta 頻段的相位-振幅耦合顯著增強。
- 相關分析顯示:
- beta2 波段功率增加 與焦慮升高幅度呈正相關。
- 額葉 alpha 不對稱指標降低幅度 與焦慮升高呈負相關。
- 前額與枕部區域 delta–beta2 PAC 增強幅度 與焦慮升高正相關。
- 結論:提供了睡眠不足導致焦慮升高的腦機制證據。
研究背景與動機
睡眠不足與焦慮:交互作用
- 睡眠剝奪 (Sleep Deprivation):現代生活常見現象(熬夜、娛樂),導致人們無法獲得充足睡眠。
- 焦慮 (Anxiety):全球常見心理問題。流行病學與實驗研究均指出,睡眠不足可能觸發或加劇狀態焦慮反應。
- 本研究以睡眠剝奪為介入模型,觀察靜息腦活動如何對應焦慮變化。
腦波頻譜:廣泛提升的假說
- 先前研究指出,睡眠剝奪後靜息態 EEG 頻譜在 delta 至 beta 波段功率皆會升高。
- delta、theta 波增加 👉 睡意上升、警覺下降。
- alpha 波提升 👉 動機與情緒調節變化。
- beta 波增強 👉 過度警覺及反芻思考。
- 高度焦慮個體在不確定情境下常出現廣泛的頻譜功率增加。本研究推測 SD 誘發的焦慮上升,可能伴隨廣泛的腦波功率增強。
額葉alpha不對稱(FAA):情緒指標
- 原理:alpha 波功率與皮質活動呈反比(alpha高 = 活性低)。
- 右側化 (Right-sided):左側活性 > 右側 👉 正向情緒、接近動機。
- 左側化 (Left-sided):右側活性 > 左側 👉 負性情緒、迴避動機、焦慮易感。
- 文獻發現 SD 後 FAA 有左側化傾向,但其與焦慮增減的關聯尚需探討。
相位-振幅耦合(PAC):跨頻溝通
- 定義:低頻波的相位與高頻波振幅之間的耦合強度。
- 低頻振盪:長距離神經溝通。
- 高頻振盪:局部神經協調。
- delta–beta 耦合:被視為情緒調節相關指標。在焦慮或不確定情境下,delta–beta PAC 會增加。
- 假設:睡眠剝奪後 delta–beta PAC 會增強(大腦更同步地處理遠距與局部訊息),並與焦慮上升呈正相關。
Question
為何關注 delta–beta PAC?
delta 波通常與睡眠壓力有關,而 beta 波與警覺/焦慮有關。 如果這兩者「耦合」在一起,是否代表大腦一邊想睡(慢波),一邊又被迫維持高度警覺(快波)的矛盾狀態?
研究方法
受試者與實驗設計
- 受試者:17 名健康年輕成人(11女6男,約19歲)。排除身心疾病,平日睡眠品質良好 (PSQI ≤ 5)。
- 實驗流程:重複測量交叉設計 (Cross-over design)。
- 正常睡眠 (NS):23:00–07:00 正常就寢。
- 睡眠剝奪 (SD):連續清醒 24 小時。
- 兩場次間隔至少一週,順序隨機。
- 測量:
- 隔日早晨進行 5分鐘眼開靜息 EEG。
- 填寫 SAI 狀態焦慮量表。
- 操作驗證:斯坦福主觀瞌睡量表 (SSS) + PVT 注意力測驗。
- EEG 處理:
- 64導聯,500Hz 取樣。
- 預處理:濾波 (0.1-80Hz)、ICA 去除偽影、分割為 2秒 epoch。
- 排除雜訊大於 ±150 µV 的區段。
指標計算
- 頻譜功率 (Spectral Power):
- 計算 delta (1–4), theta (4–7), alpha (8–13), beta1 (13–20), beta2 (20–30) 各頻段平均功率。
- 比較 SD vs. NS 差異。
- 額葉alpha不對稱 (FAA):
- 公式:
- 下降 = 左側化(左側 alpha 功率相對增加 / 右側額葉活性相對下降)。
- 相位-振幅耦合 (PAC):
- 關注 delta–beta1 與 delta–beta2。
- 方法:平均向量長度 (MVL-MI)。
- 公式:
- 分析 PAC 改變量 (SD-NS) 與焦慮改變量 (deltaSAI) 的相關性。
實驗結果與主要圖表
1. 主觀狀態焦慮與操作驗證
- 焦慮升高:SD 後 SAI 分數顯著高於 NS ( p < 0.05 )
- 有效性:SD 後睡意顯著增強 (SSS),警覺反應變慢 (PVT)。
- 腦波頻譜:SD 導致 全頻段 (delta, theta, alpha, beta1, beta2) 功率皆顯著升高,符合皮質興奮性提高及高焦慮特徵。 👉 Insomnia則會導致delta下降,剩下theta, alpha, beta1, beta2升高
2. 額葉 alpha 波不對稱:左側化
- FAA 顯著下降:從 NS 的正值 () 轉為 SD 的負值 ()。
- 意義:呈現 左側化 (Left-sided) 優勢 👉 迴避/退縮動機增強。
- 相關性:FAA 降低幅度與 SAI 升高幅度呈顯著負相關 ()。
- 越左側化(FAA降越多),焦慮增加越多。
3. delta–beta PAC:耦合增強與焦慮關聯
- PAC 增強:SD 後 delta–beta PAC 顯著高於 NS。
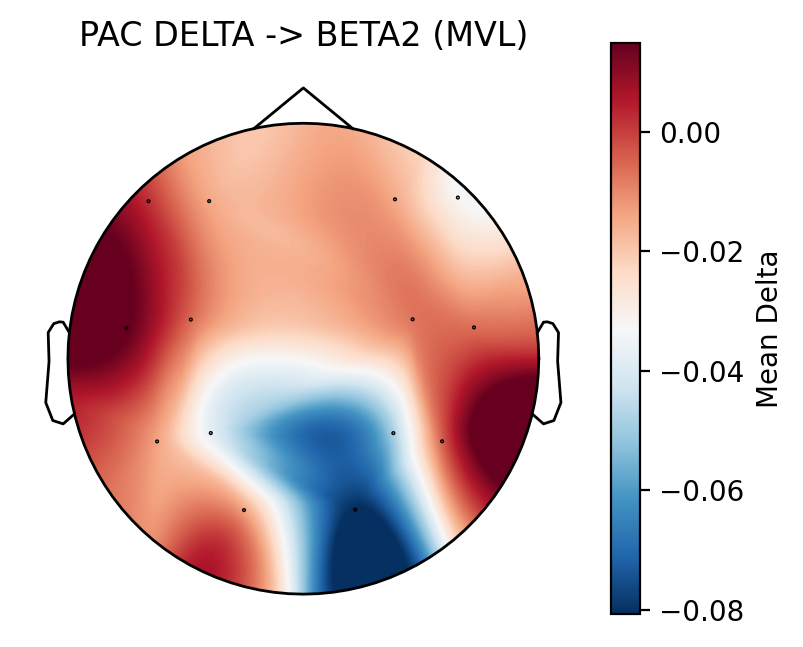
- 最明顯頻段:delta–beta2 (20–30 Hz)。
- 顯著區域:中央區電極 (FDR 校正顯著)。
- 生理意涵:大腦同時累積大量慢波(睡眠壓力)與快波(焦慮警醒),且兩者同步性加強。
- 相關性:
- delta–beta2 PAC 增強幅度 與 SAI 升高量呈顯著正相關。
- 關鍵區域:額區前極 (FP1, Fz…) 與 枕區 (Oz, O1…)。
- 例如 Fz 電極相關係數 。
- 推論:慢波促進遠距整合,快波負責威脅偵測;兩者協調提高代表個體處於高度警戒狀態。
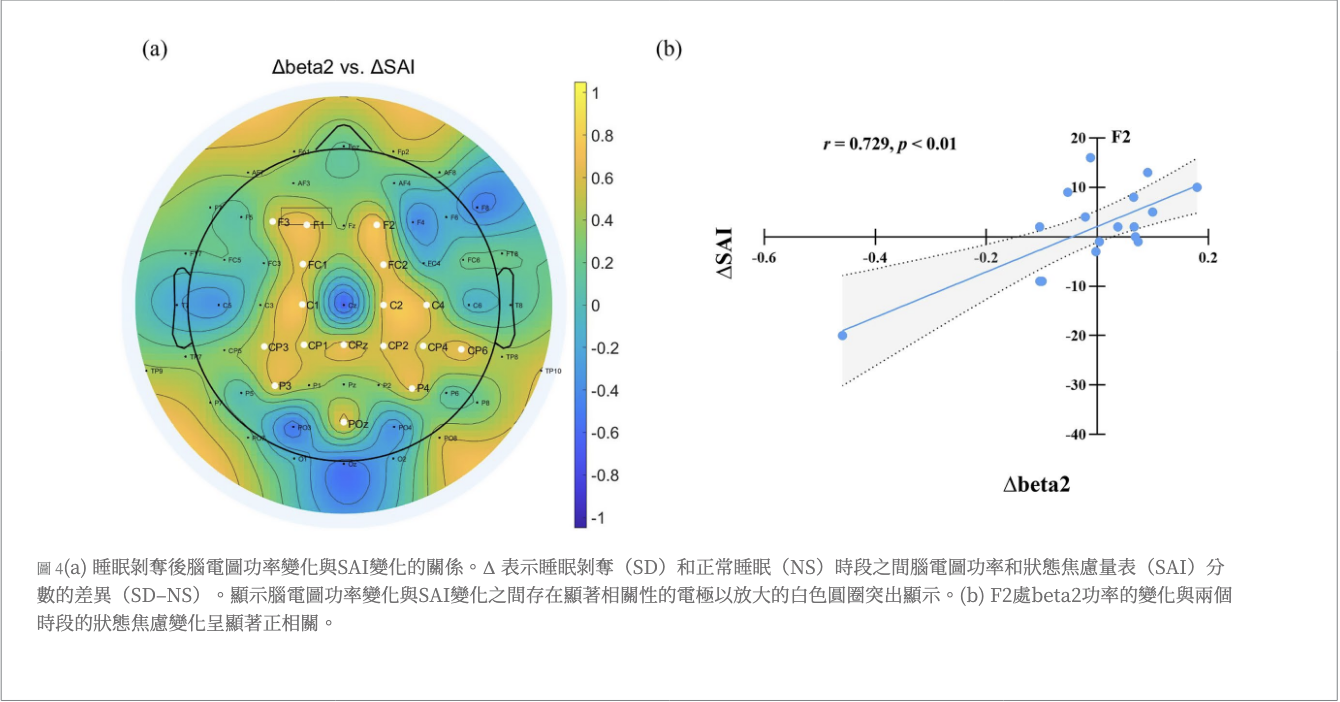 圖說:(a) deltaPAC 與 deltaSAI 相關分布,白圈為顯著區域(額/枕區);(b) Fz 電極散點圖顯示正相關。PAC 增強越明顯,焦慮提升越多。
圖說:(a) deltaPAC 與 deltaSAI 相關分布,白圈為顯著區域(額/枕區);(b) Fz 電極散點圖顯示正相關。PAC 增強越明顯,焦慮提升越多。
討論與總結
核心發現:大腦進入「高警戒空轉」狀態
一晚睡眠剝奪後,大腦呈現多層次改變:
- 全頻譜功率上升:皮質去喚醒 (de-arousal),神經元興奮但功能空轉。
- FAA 左側化:威脅敏感度提高,傾向採取迴避策略。
- delta–beta PAC 增強:威脅訊息處理的協同性增加,大腦處於備戰狀態。
指標臨床意義
- FAA:作為評估缺睡對情緒調節影響的簡便生理指標。
- PAC:連結睡眠生理與情緒狀態的橋樑。即使是健康人,急性缺睡也會出現類似焦慮症的耦合增強。
比較:急性缺睡 vs. 慢性失眠 (Insomnia)
本研究針對急性 SD,但這與慢性失眠的神經特徵可能截然不同。
| 比較維度 | 健康對照組 (HC) / 本研究 SD 前 | 本研究:急性睡眠剝奪 (Acute SD) | 慢性失眠患者 (Chronic Insomnia) |
|---|---|---|---|
| 狀態 | 平衡 | 高壓警戒 | 長期失調 |
| 低頻波 (Delta/Theta) | 節奏分明的指揮官 | 暴增 (睡眠壓力) | 指揮力弱,訊號混亂 |
| 高頻波 (Beta/Gamma) | 特定時刻出現 | 暴增 (焦慮警覺) | 持續存在,分佈雜亂 |
| PAC 耦合強度 | 高且規律 (有效溝通) | 異常增強 (過度同步/備戰) | 低/散亂 (溝通斷裂) |
| 生理意義 | 放鬆/睡眠品質佳 | 焦慮激增,大腦超負荷 | 大腦「待機」,無法深睡 |
Note
Note: 急性缺睡因壓力反應導致慢-快波同時大量出現並強烈耦合;而慢性失眠則因長期高覺醒導致慢波受阻、跨頻協調能力下降。兩者雖然都伴隨焦慮,但神經機制可能相反。
結論與貢獻
本研究證明了睡眠不足如何透過改變大腦的振盪互動模式(特別是 delta–beta PAC 和 FAA)來誘發焦慮。 Hao 等人(2025)的研究強化了「良好睡眠是情緒穩定的基石」:不論是偶發的一夜不眠,還是長期的失眠,睡眠質量的下降都深刻改變了大腦的情緒調節機制。PAC 有潛力作為未來評估睡眠障礙與焦慮風險的精準生物標記。
- 提升幅度圖